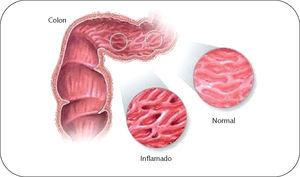
Enfermedad inflamatoria intestinal. Terapia nutricional
Share
La enfermedad inflamatoria intestinal incluye un grupo de enfermedades crónicas que, además de afectar al intestino y a otros órganos, se han relacionado con la nutrición por diferentes vías. En el presente artículo se revisan las repercusiones, en el ámbito nutricional, de esta entidad clínica, así como las opciones terapéuticas disponibles también en este terreno.
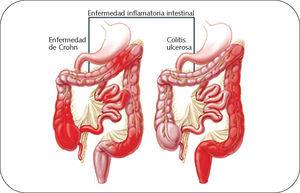
Con la denominación de enfermedad inflamatoria intestinal (EII) se agrupan distintos procesos inflamatorios crónicos, cuya etiología es desconocida. Entre esos procesos destacan la enfermedad de Crohn y la colitis ulcerosa. La enfermedad de Crohn afecta fundamentalmente al íleon terminal, al colon y al ano, mientras que la colitis ulcerosa se localiza básicamente en el recto y en el colon distal, si bien puede extenderse proximalmente a todo el colon (fig. 1).
Fig. 1. Enfermedad inflamatoria intestinal
La colitis ulcerosa es una enfermedad inflamatoria localizada fundamentalmente en el intestino grueso, cuyo inicio tienen lugar en el recto, donde da lugar a la denominada proctitis ulcerosa. A partir de ahí el proceso inflamatorio se extiende de forma continua y simétrica pudiendo afectar a otros segmentos del colon y generando las denominadas proctosigmoiditis, colitis ulcerosa izquierda, colitis ulcerosa extensa y pancolitis ulcerosa. La afectación está limitada a la mucosa y submucosa intestinal, sin dañar la capa muscular.
Clínica
La enfermedad de Crohn puede estar localizada en cualquier parte del tubo digestivo, desde la boca hasta el ano, aunque normalmente suele aparecer en íleon distal y colon ascendente. El proceso inflamatorio es discontinuo y asimétrico. A diferencia de la colitis ulcerosa (fig. 2), donde la inflamación es de tipo ulcerativo, en la enfermedad de Crohn el proceso inflamatorio es de tipo granulomatoso y transmural, afectando en grados variables a toda la pared intestinal, lo que puede acarrear estenosis y fístulas intraabdominales o perianales, así como abscesos abdominales.
Fig. 2. Colitis ulcerosa frente a enfermedad de Crohn
Actualmente se piensa que la colitis ulcerosa y la enfermedad de Crohn son enfermedades de causa multifactorial, con base genética y clínica heterogéneas, que presentan signos morfológicos superpuestos, si bien hay aspectos que las diferencian.
Ambas enfermedades suelen evolucionar en brotes o recidivas de gravedad variables seguidos de períodos de remisión; hay que resaltar que su curso es impredecible. Casi el 50% de los pacientes presenta un brote de actividad al año.
Patogenia
En relación con la patogenia de la enfermedad, se admite que además de los factores genéticos, hay factores desencadenantes adicionales, los denominados precipitantes ambientales y los cofactores de la enfermedad. En este sentido, un factor precipitante sería una infección por un determinado patógeno, unida a una función defectuosa de la barrera intestinal, que desencadenaría una respuesta inflamatoria crónica en individuos genéticamente predispuestos con trastornos en la regulación del sistema inmunitario. La flora intestinal es un requisito, y posiblemente un factor central, para el desarrollo de enfermedad inflamatoria intestinal; en este sentido, algunos agentes infecciosos como Mycobacterium paratuberculosis parecen aliviar el proceso de base mantenido por las bacterias intestinales comensales.
Entre los desencadenantes ambientales de la enfermedad inflamatoria intestinal se ha valorado el posible papel que puede tener la alimentación, si bien hay que decir que los diferentes estudios llevados a cabo hasta la fecha no han aportado resultados concluyentes.
Como se ha mencionado con antelación, ambas enfermedades evolucionan con períodos de remisión y agudización, que se alternan cíclicamente. Desde el punto de vista clínico, la enfermedad de Crohn y la colitis ulcerosa se caracterizan por la presencia de diarrea, dolor abdominal, pérdida de peso, hemorragia rectal y fiebre, síntomas estos que presentan distinta intensidad en una y otra afección. Así, mientras que en la enfermedad de Crohn el dolor abdominal es un síntoma constante, en la colitis ulcerosa predomina la hemorragia rectal.
Junto a estas manifestaciones, hay otras de carácter extraintestinal, debidas a la presencia de inmunocomplejos circulantes, lo que podría apoyar la teoría inmunológica barajada en la etiopatogenia de la enfermedad. Estas manifestaciones incluyen trastornos osteoarticulares (artritis, espondilitis, etc.), cutáneos (eritema nudoso), oculares (uveítis, conjuntivitis) o nefrourológicos (nefrolitiasis).
Las principales complicaciones son el megacolon tóxico (fig. 3) y la perforación del colon en la colitis ulcerosa, y las fisuras, fístulas y estenosis en la enfermedad de Crohn.
EII y estado nutricional
La enfermedad inflamatoria intestinal se encuentra relacionada con la nutrición por diferentes aspectos:
Alta prevalencia de malnutrición energeticoproteica y otras deficiencias nutricionales en pacientes que sufren enfermedad inflamatoria intestinal.
Diferente incidencia de enfermedad inflamatoria intestinal en relación con distintos hábitos dietéticos poblacionales, lo que sugiere que algunos nutrientes pueden tener un papel patogenético en el desarrollo de la enfermedad.
La intervención nutricional parece tener un efecto terapéutico primario en algunos subgrupos de pacientes.
Malnutrición energeticoproteica y EII
La malnutrición energeticoproteica es un rasgo importante de la enfermedad inflamatoria intestinal. Afecta aproximadamente a una proporción de enfermos comprendida entre el 20-80%. Esta amplia variación es debida a la heterogeneidad de los estudios publicados, así como a las diferentes formas en cuanto a gravedad y extensión de la enfermedad. Si bien la malnutrición energeticoproteica es más frecuente en pacientes con enfermedad activa hospitalizados, también puede observarse en pacientes ambulatorios, sobre todo en la colitis ulcerosa crónicamente activa, que requiere tratamiento esteroide continuado.
El desarrollo de malnutrición ocurre en gran medida como consecuencia de la respuesta inflamatoria local y sistémica. En este sentido, la inflamación origina un estado de ineficacia anabólica, caracterizado por disminución de la síntesis proteica, particularmente en el sistema musculoesquelético, unido a un mayor catabolismo proteico en tejido conectivo y musculoesquelético. Al mismo tiempo se produce anorexia como consecuencia de la actividad aumentada del factor de necrosis tumoral alfa y de la interleucina-1.
La malnutrición energeticoproteica es debida fundamentalmente a la anorexia de los pacientes y a la restricción de la ingesta alimentaria que realizan tratando de aliviar los síntomas intestinales de la enfermedad. En general, se admite que la contribución de la malabsorción a los cuadros de malnutrición puede dar lugar a graves cuadros de desnutrición.
En la enfermedad de Crohn, los brotes de actividad suelen ser más crónicos y menos intensos, lo que hace que la malnutrición se instaure de forma insidiosa y sea de tipo mixto, energeticoproteica. La colitis ulcerosa se caracteriza por brotes agudos de mayor intensidad, lo que se traduce en que la malnutrición, de predominio proteico visceral, se desarrolle de forma más rápida.
El peso corporal, los parámetros nutricionales antropométricos, la determinación de las diferentes proteínas viscerales, la fuerza de compresión del puño, las determinaciones de vitaminas y minerales, así como la densitometría ósea, han sido los métodos más frecuentemente utilizados para evaluar la malnutrición energeticoproteica. No obstante, la hipoalbuminemia constituye un hallazgo frecuente en los brotes de actividad de enfermedad inflamatoria intestinal.
Deficiencia vitaminicomineral y EII
En los pacientes con enfermedad inflamatoria intestinal, las deficiencias de micronutrientes con actividad antioxidante (carotenos, vitaminas A, C y E, selenio y cinc) son particularmente intensas y evidentes.
Si bien la deficiencia de micronutrientes se manifiesta clínicamente en muy pocas ocasiones, sus consecuencias son relevantes. En este sentido, es de sobra conocido que la deficiencia de micronutrientes antioxidantes disminuye las defensas frente al estrés en ciertas patologías en las que éste se encuentra claramente aumentado.
La malabsorción de sales biliares en el íleon distal puede generar esteatorrea, malabsorción de vitaminas liposolubles y mayor eliminación fecal de ciertos minerales. En concreto, la deficiencia más frecuente de vitaminas liposolubles es la deficiencia de vitamina D.
Desnutrición y EII
Una de las principales complicaciones de la enfermedad inflamatoria intestinal está originada por las alteraciones nutricionales, ya que repercuten intensamente en el organismo e influyen negativamente en el curso de la enfermedad.
Pérdida de peso corporal, retraso del crecimiento y del desarrollo, anemia, astenia, edema, calambres musculares, diarrea, debilitamiento de la inmunidad celular, y como manifestación tardía, enfermedad metabólica ósea, son las manifestaciones clínicas de la malabsorción en la enfermedad inflamatoria intestinal. La diarrea puede ponerse de manifiesto debido a deficiencias de ácido fólico, vitamina B12, niacina, cinc y proteínas.
En pacientes con enfermedad inflamatoria intestinal, la frecuencia de fenómenos tromboembólicos está aumentada, lo cual puede atribuirse al efecto procoagulante de las citoquinas proinflamatorias, aunque también se han relacionado con la hiperhomocisteinemia, cuyo origen habría que buscarlo en deficiencias nutricionales de ácido fólico, vitamina B12 y piridoxina.
Otro de los problemas que presentan los pacientes con enfermedad inflamatoria intestinal, y especialmente con enfermedad de Crohn, es el retraso del crecimiento, cuyo origen es de carácter multifactorial. Está implicada la actividad inflamatoria de la enfermedad, la desnutrición persistente y el tratamiento con glucocorticoides.
Finalmente, en cuanto a la influencia sobre la evolución de la enfermedad, la malnutrición se relaciona con los siguientes problemas:
Dificultad para la reparación y la cicatrización de los tejidos lesionados, así como para la curación de las fístulas.
Inhibición de las funciones del tracto gastrointestinal.
Deficiencia en el transporte plasmático de fármacos.
Mayor riesgo quirúrgico.
Aumento de la morbilidad perioperatoria.
Manejo nutricional de la EII
La frecuencia con que se presentan problemas nutricionales y sus consecuencias ha motivado que la terapia nutricional intervenga de manera importante en el tratamiento de la enfermedad inflamatoria intestinal. Los objetivos nutricionales en esta enfermedad consisten en mantener o recuperar un estado nutricional correcto, ya que tanto la colitis ulcerosa como la enfermedad de Crohn son procesos con un elevado riesgo de desnutrición. Obviamente, las recomendaciones dietéticas hacen un especial énfasis en reemplazar la pérdida de nutrientes asociada al proceso inflamatorio y corregir las deficiencias subsiguientes. Las recomendaciones deben evitar el agravamiento de los síntomas y/o su aparición, aunque debe intentarse que la dieta sea equilibrada y apetecible para el enfermo, huyendo de las restricciones que no sean necesarias. Por último, en algunos pacientes puede ser necesario el tratamiento primario con nutrición enteral para inducir la remisión del brote de actividad en la enfermedad de Crohn.
En los pacientes con mayor riesgo de desnutrición, entre los que se incluyen aquellos que están en situación de brote agudo de intensidad moderada o grave, presentan enfermedad de Crohn de larga evolución, con afectación intestinal extensa, con complicaciones como estenosis o resecciones de intestino delgado, así como en los que realizan dietas restrictivas, se debe hacer un seguimiento de la ingesta alimentaria y monitorizar sistemáticamente los indicadores nutricionales necesarios para detectar las deficiencias nutricionales asociadas a cada una de las situaciones que se acaban de comentar y evaluar la eficacia de la intervención terapéutica nutricional.
Conviene no olvidar que también durante las fases de inactividad de la enfermedad inflamatoria intestinal pueden presentarse problemas nutricionales, debidos en algunos casos a la prescripción de dietas demasiado restrictivas. Hasta la fecha no disponemos de evidencia científica de que algún alimento concreto se asocie con recidivas de la enfermedad, por lo que al paciente con enfermedad inflamatoria intestinal debe aconsejársele que siga una dieta libre. Se ha comprobado que casi la mitad de los enfermos con colitis ulcerosa tienen ideas preconcebidas respecto a la alimentación; en este sentido, es frecuente que asocien los productos lácteos y los alimentos ricos en fibra con una agudización de la enfermedad, creencias éstas que no han podido ser demostradas, pero que, sin embargo, sí han originado una mayor pérdida de densidad mineral ósea en aquellos enfermos que las han puesto en práctica.
El tratamiento nutricional es un componente fundamental del manejo terapéutico global de las personas con enfermedad inflamatoria intestinal, principalmente como terapia complementaria, aunque en algunos casos seleccionados de enfermedad de Crohn también puede utilizarse como tratamiento primario para inducir la remisión del brote de actividad.
Tratamiento dietético
En primer lugar, se realizará una valoración nutricional con el fin de determinar el estado del paciente y estimar sus necesidades.
Los resultados de un estudio de Stokes y Hill (1993) que determinó el gasto energético total para estos enfermos indicaban que dicho valor oscilaba entre 30-35 kcal/kg/día, de los cuales el 70% era debido al gasto energético basal, el 10% a la termogénesis inducida por los alimentos y el 20% al índice de actividad física. Los requerimientos proteicos pueden variar de 1-2 g/kg/día, en función de la gravedad de la enfermedad, de la pérdida de proteínas a través del tracto digestivo, etc.
Realmente es difícil establecer normas dietéticas y nutricionales de carácter general en la enfermedad inflamatoria intestinal. Ello es debido a que tanto la intensidad como la tolerancia alimentaria son variables que dependen de la entidad patológica (enfermedad de Crohn o colitis ulcerosa), su extensión y localización, así como de la existencia o no de resección intestinal previa. Esto obliga a individualizar las recomendaciones dietéticas.
Por otra parte, aquellos pacientes que estén atravesando un brote activo de la enfermedad inflamatoria intestinal pueden sufrir un empeoramiento en sus síntomas digestivos cuando realizan una ingesta por vía oral. Ello es debido a que se produce un aumento en la cantidad de líquido y residuos no digeribles que transitan por el intestino delgado y alcanzan el colon; al mismo tiempo, si se elimina la ingesta oral, disminuyen las actividades peristáltica y secretora del intestino. Si bien en un principio, cuando se utilizó nutrición parenteral previa a la cirugía en pacientes con enfermedad de Crohn, se observó que en algunos casos se alcanzaba la remisión clínica y se evitaba una intervención ya programada --lo que hizo pensar que la nutrición parenteral, además de su efecto nutricional, podía aportar un efecto primario al conseguir la remisión del brote de actividad--, actualmente se admite que este tipo de nutrición, combinado con el reposo intestinal, no proporciona ventajas en comparación con la utilización de la vía digestiva en la inducción de remisiones clínicas en la enfermedad inflamatoria intestinal. De ahí que, hoy por hoy, la dieta absoluta como tratamiento primario de la enfermedad de Crohn o de la colitis ulcerosa esté desaconsejada. No obstante, si el brote de actividad se complica y aparece el megacolon tóxico, la dieta absoluta es una medida que obligatoriamente hay que pautar.
Las principales recomendaciones dietéticas aplicables a pacientes con brote agudo moderado o grave que se encuentren ingresados son las siguientes:
La dieta absoluta está desaconsejada.
La dieta contendrá inicialmente alimentos de fácil digestión y absorción, evitándose la fibra insoluble y los lácteos, a excepción del yogur.
A medida que se produzca una mejora en el apetito y en los síntomas digestivos del enfermo, se intentará introducir una alimentación rica en proteínas y con suficiente energía, adaptada obviamente a la tolerancia y a las preferencias alimentarias del paciente.
Se introducirán las modificaciones y las restricciones alimentarias para prevenir y/o tratar complicaciones asociadas, entre las que se incluyen esteatorrea, estenosis ileal y síndrome de intestino corto.
Los suplementos orales pueden ser necesarios en algunos pacientes con objeto de completar su ingesta energética y proteica. En los pacientes que no estén ingresados, el principal consejo dietético ha de centrarse en la necesidad de que ingieran una alimentación rica en proteínas, y con las calorías suficientes para mantener o restaurar el peso corporal, y en el caso de niños y adolescentes, permitir un adecuado crecimiento.
Un grupo de alimentos que resulta especialmente controvertido en pacientes con enfermedad inflamatoria intestinal es el de los productos lácteos. Se ha comprobado que algunos pacientes con enfermedad inflamatoria intestinal presentan también deficiencia de lactasa, pero dicha deficiencia no es mayor en pacientes con enfermedad inflamatoria intestinal que en población general. Usualmente los sujetos con deficiencia de lactasa toleran mejor el yogur que la leche, ya que el primero posee menos cantidad de lactosa que el segundo.
Finalmente, si el paciente está en fase de remisión de la actividad inflamatoria, puede perfectamente llevar a cabo un plan de comidas apetitoso y saludable, introduciendo las restricciones dietéticas única y exclusivamente en aquellos casos en los que haya que tratar complicaciones asociadas.
La malnutrición energeticoproteica es un rasgo importante de la enfermedad inflamatoria intestinal y afecta aproximadamente a una proporción de pacientes comprendida entre el 20 y el 80%
Tratamiento con nutrición artificial
La nutrición artificial, entendida ésta como la administración de fórmulas definidas de nutrientes por vía oral, gastrointestinal o parenteral, se plantea como tratamiento complementario con las siguientes indicaciones:
Prevenir la desnutrición.
Restaurar la normalidad del estado nutricional en caso de desnutrición.
Promover el crecimiento en los niños con retraso a este respecto.
Tratamiento primario en casos concretos para inducir la remisión del brote de actividad inflamatoria en pacientes con enfermedad de Crohn.
La elección de nutrición enteral o parenteral en pacientes con enfermedad inflamatoria intestinal dependerá de la situación clínica del enfermo, si bien cuando las condiciones lo permitan, se elegirá la nutrición enteral, ya que por fisiología, seguridad y coste económico es la más adecuada.
La nutrición enteral permite realizar un aporte de nutrientes parcial o completo. La vía de administración puede ser por vía oral, por sonda o por ostomía. La fórmula a elegir dependerá de la capacidad funcional del tracto gastrointestinal, reservándose las fórmulas elementales y las oligoméricas para pacientes con función intestinal alterada y marcada disminución de las capacidades digestiva y absortiva. Habitualmente las fórmulas más recomendadas son las poliméricas que, en general, resultan bien toleradas y tienen mejor sabor que las elementales de cara a su administración por vía oral. Otra de sus ventajas frente a las fórmulas elementales y las oligoméricas es que permiten administrar mayor cantidad de nitrógeno.
Si las necesidades energéticas y proteicas no se cubren mediante la nutrición enteral, habrá que recurrir a la nutrición parenteral, la cual también están indicada en las siguientes situaciones: peritonitis difusa, íleo paralítico, obstrucción intestinal completa, isquemia intestinal, hemorragia digestiva aguda, perforación intestinal, vómitos incoercibles, diarrea masiva, fístulas entéricas proximales de alto débito, fase inicial del síndrome de intestino corto y megacolon tóxico.
Mención especial merece la nutrición enteral como tratamiento primario de la enfermedad de Crohn, cuya utilidad en esta condición fue descubierta casualmente al comprobar que aquellos pacientes que recibían sólo fórmulas elementales para mejorar su estado nutricional con objeto de ser intervenidos quirúrgicamente experimentaban una mejoría en la actividad inflamatoria intestinal. Su uso en estos enfermos se ha prolongado durante más de 30 años ya que, además de reducir la inflamación intestinal, tiene pocos efectos adversos y mejora el estado nutricional, así como el crecimiento.
Durante los últimos años se ha estudiado ampliamente el mecanismo por el que se produce este efecto primario. Inicialmente se planteó que las dietas ricas en aminoácidos podían ser especialmente útiles dada su baja antigenicidad, sin embargo, los resultados de un metaanálisis de estudios que comparaban dietas elementales y dietas no elementales no han confirmado esta hipótesis. Según dichos estudios, el efecto terapéutico de la nutrición enteral en la enfermedad de Crohn no depende del tipo de fuente nitrogenada que se administre.
También se ha sugerido que la cantidad y el tipo de grasa de la dieta enteral podían ser los responsables del efecto primario de ésta. En este sentido se ha señalado que las dietas con bajo contenido lipídico triglicéridos de cadena larga-- obtienen tasas de remisión mucho más altas que cuando se administran dietas con alto contenido graso.
Alimentos funcionales en la EII
La eficacia de la nutrición enteral para provocar la remisión de los brotes de actividad en la enfermedad de Crohn, especialmente cuando se utilizan como única fuente alimentaria, induce a pensar que alguno de los componentes de la alimentación convencional interviene en la patogenia de la enfermedad. Algunos mecanismos propuestos apuntan hacia la importancia de la composición nutricional de las fórmulas, al efecto farmacológico de los nutrientes o, incluso, a factores no nutricionales. Se ha especulado con la posibilidad de que las remisiones de la enfermedad de Crohn activa estén relacionadas con los siguientes factores:
Disminución de la carga antigénica en el intestino.
Disminución de la síntesis de mediadores inflamatorios intestinales.
Provisión de nutrientes importantes para la reparación de las lesiones intestinales.
Actividad de nutrientes antioxidantes.
Es evidente que todos estos factores están íntimamente ligados a la actividad de los diferentes alimentos funcionales. En este sentido, hay bastante información sobre la eficacia de distintos nutrientes para tratar la enfermedad inflamatoria intestinal: probióticos, cantidad de triglicéridos, clase de ácidos grasos, fuente de nitrógeno, cantidad de glutamina, vitaminas antioxidantes, prebióticos y otros factores tales como citoquinas antiinflamatorias y micropartículas; sin embargo, hay muy poca evidencia sobre la utilidad de los factores citados en el tratamiento de la enfermedad inflamatoria intestinal.
Por otra parte, el funcionamiento del colon depende fundamentalmente de la presencia de nutrientes en su luz que permiten el mantenimiento de su trofismo y funciones, así como una homeostasis bacteriológica en la flora que contiene. Diferentes sustratos nutritivos alcanzan el colon y entran en contacto con la flora bacteriana intestinal, conformando un verdadero organismo metabólico compuesto por más de 104 colonias de bacterias/mm3 de contenido colónico. La metabolización de estos productos es esencial para mantener la estructura y función del intestino grueso. Cuando las bacterias anaerobias del colon fermentan los hidratos de carbono no absorbidos, se generan gases y ácidos grasos de cadena corta que actúan como un combustible esencial para el colonocito, de tal manera que su deficitaria oxidación favorece el desarrollo de procesos inflamatorios en el colon.
Si se parte de la base de que la enfermedad inflamatoria intestinal se desarrolla como respuesta a la flora intestinal, la modificación de dicha flora podría tener efectos terapéuticos. En este punto entrarían en juego los probióticos y los prebióticos, que se convertirían así en recursos terapéuticos útiles para influir en el complejo ecosistema bacteriano del intestino, sin los efectos adversos propios de los antibióticos.
En relación con los probióticos, se han llevado a cabo estudios con la mezcla VSL#3 con 4 cepas de lactobacilos (Lactobacillus casei, L. plantarum, L. acidophilus y L. delbrueckii subesp. bulgaricus), 3 cepas de bífidobacterias (Bifidobacterium longum, B. breve y B. infectis) y una cepa de Streptococcus salivarius subesp. termophillus. Los estudios preliminares sugieren que este preparado es efectivo para mantener la remisión en pacientes con colitis ulcerosa, aunque se requieren nuevos y mejores estudios para aportar evidencia científica que corrobore la utilidad de estos preparados.
Otro camino para promover el crecimiento de bacterias probióticas es la ingestión de componentes dietéticos que favorezcan su desarrollo. Se trata de los denominados prebióticos, que, junto con algunos tipos de fibra fermentable no alimentaria (semillas de Plantago ovata) y precursores de ácidos grasos de cadena corta, podrían contribuir a la reparación de la mucosa del colon y del intestino delgado distal, ya que estos ácidos grasos, además de ser nutrientes específicos del epitelio intestinal, disminuyen la inflamación. Al mismo tiempo, la composición de la flora colónica es modulada por los prebióticos, disminuyendo el pH intraluminal y favoreciendo la proliferación de bacterias acidolácticas probióticas e inhibiendo la de otras, incluidas probablemente algunas con potencial patógeno.
En resumen, puede decirse que el empleo de productos funcionales para tratar la enfermedad inflamatoria intestinal pertenece todavía al campo de la experimentación, siendo necesarios más estudios que aporten la evidencia científica suficiente para recomendar su empleo como tratamiento primario en la enfermedad inflamatoria intestinal.
Etiología
Si bien se desconoce su etiología, se cree que los fenotipos de la enfermedad resultan de complejas interacciones entre factores genéticos, inmunorreguladores y ambientales; se supone que estas interacciones activan exagerada y continuamente la respuesta inmunitaria en la mucosa intestinal. Al parecer, la susceptibilidad genética para desarrollar la enfermedad inflamatoria intestinal podría heredarse de forma poligénica compleja y en la enfermedad de Crohn este componente parece ser más importante que en la colitis ulcerosa.
Bibliografía general
Arrizabalaga JJ. Manejo nutricional de la enfermedad inflamatoria intestinal. Endocrinología y Nutrición. 2007;3:151-8.
Cabre E, Gassull MA. Nutrición en la enfermedad inflamatoria intestinal. En: Gil A, Álvarez J, García de Lorenzo A, Montejo JC, Planas M (eds.). Tratado de Nutrición, tomo IV. Madrid: Acción Médica; 2005. p. 880-906.
Casamitjana N. Enfermedad inflamatoria intestinal. Colitis ulcerosa y enfermedad de Crohn. Farmacia Profesional. 1999;4:68-70.
Cuerda MC, Breton I, Camblor M, García Peris P. Soporte nutricional basado en la evidencia en la enfermedad inflamatoria intestinal. En: Bellido D, Ballesteros MD, Álvarez J, del Olmo D (eds.). Nutrición basada en la evidencia. Endocrinología y Nutrición. 2005;Supl. 2:70-7.
Fernández F, Gassull MA. Revisión y consenso en terapia nutricional: nutrición en enfermedad inflamatoria intestinal. Nutrición Hospitalaria. 1999;Supl. 2:71S-80S.
García R. Enfermedad inflamatoria intestinal. Guías clínicas 2003, (consultado el 2 de abril de 2007). Disponible en: http://www.fisterra.com/guias2/eii.asp
García P, Camblor M, de la Cuerda C, Breton I. Recomendaciones nutricionales en la enfermedad inflamatoria intestinal. En: León M, Celaya S (eds.). Manual de Recomendaciones Nutricionales al Alta Hospitalaria. Madrid: You&US; 2001. p. 45-8.
González-Huix F. Enfermedad inflamatoria intestinal. Trastornos nutricionales y su repercusión. GETECCU (Grupo español de trabajo en enfermedad de Crohn y colitis ulcerosa) y FAES Farma SA. 2004, (consultado el 25 de abril de 2007). Disponible en: http://www.faes.es/archivos_pdf/dowland/bases_bibliograficas/eii/EII_01.PDF
Sebastián JJ. Enfermedad inflamatoria intestinal. Revisión. Farmacia Profesional. 2000;6:84-94.
Stokes MA, Hill GL. Total energy expenditure in patients with Crohn's disease: measurement by the combined body scan technique. JPEN. 1993;1:3-7.Ç